il costellos
Transkript
Hmotnostní spektrometrie Petr Man [email protected] Unikátní vlastnosti hmotnostní spektrometrie Specifita Rychlost Jednoduchá interpretace dat Citlivost Čísla k zapamatování (1 mol ~ 6.023 x 1023 molekul) molekul molů 10-9 1 zrnko soli ~ 1 ug ~ 20 nmol 1015 1-10 pmol pro CBB 1 pmol pro Edmanovo odb. 100 fmol pro stříbrem barvené gely 1012 10-15 2 fmol: jedna kopie v 109 buněk 109 10-17 10 amol: ICR FTMS 106 10 zmol: Iontová past (300-1000 iontů) 103 10-12 10-21 Hmotnostní spektrometr Normální tlak Vložení vzorku Snížený tlak Ionizační technika Hmotnostní analyzátor Detektor Počítač • Měříme pseudomolekulární ionty v plynné fázi (M-H+, M+H+, M+Na+, atd.) • Jak spočítáme M? – nejlépe z elementárního složení. http://medlib.med.utah.edu/masspec/mole.htm • Monoisotopická vs. Průměrná MW C6H12O6 Mmono = 180.0633; Mavg = 180.1576 C113H171N27O31S1 Mmono = 2434.2354 ; Mavg = 2435.8301 Přítomnost izotopů (13C, 15N, 17O, …) se projeví na tvaru píku. 13C je 1.1%, tj. na každých 100 uhlíků je jeden 13C více uhlíků -> více 13C, to se projeví na tvaru píku Intenzita druhého izotopu je 1.1xpočetC – získáme % intenzity prvního píku. Máme ale i další izotopy… Kouzla s izotopy Ionizační metody • EI – Electron Impact • CI – Chemical Ionization • APCI / APPI – Atmospheric Pressure – Chemical Ionization / Photo Ionization • FD – Field Desorption • PD – Plasma Desorption • FAB – Fast Atom Bombardment • ESI / nanoESI – ElectroSpray Ionization • MALDI – Matrix Assisted Laser Desorption/Ionization 1985 Elektrosprej – J. B. Fenn 1994 – nanoelektrosprej – M. Mann a M. Wilm Fenn JB; Mann M; Meng CK; Wong SF; Whitehouse CM: Science 1989, 246, 64. Ionizace elektrospejem Rozpouštědlo/Pufr + + ESI Jehla (5 kV) + + Vstupní Vyhřívaná otvor kapilára (0-50 V) + ++ + + Iontový Svazek Ionizace elektrosprejem • Velmi měkká ionizace • Mnohonásobně nabité ionty – 1, 2, 3, …60x • Malá nebo téměř žádná fragmentace • proteiny, peptidy, oligosacharidy, nukleotidy, syntetické polymery ... • Nekovalentní komplexy (proteinové komplexy, komplexy protein-ligand, atd.) • Vhodná pro kvantifikaci • Vysoká náročnost na čistotu • Napojitelné na LC • Spojení s jakýmkoliv analyzátorem 1987 – Desorpce laserem za přítomnosti matrice K. Tanaka / M. Karas, F. Hillenkamp Karas M; Bachmann D; Bahr U; Hillenkamp F: Int. J. Mass Spectrom. Ion Proc. 1987, 78, 53. Tanaka K; Waki H; Ido Y; Akita S; Yoshida Y; Yoshida T: Rapid Commun. Mass Spectrom. 1988, 2, 151. MALDI Ionizační proces MALDI Ionizační proces MALDI matrice dobrá absorpce za použité vlnové délky stabilita ve vakuu, netěkavá přenos protonu 2,5-DHB vzorek : matrice = 1 : 104-105 mísitelné se vzorkem v tuhé fázi solventy: MeOH, EtOH, MeCN, H2O, THF, aceton ... UV-MALDI 337 nm dusíkový laser 355 nm Nd:YAG 266 nm Nd:YAG 193 nm ArF IR-MALDI 2.94 mm Er:YAG laser 10.6 mm CO2 laser MALDI matrice kys. 2,5-dihydroxybenzoová (DHB) kys. sinapová (SA) (kys. 3,5-dimethoxy-4-hydroxyskořicová) kys. α-kyano-4-hydroxyskořicová (CCA) kys. ferulová (FA) (kys. 4-hydroxy-3-methoxyskořicová) MALDI Ionizační proces • Měkká ionizace • Malá nebo žádná fragmentace, jednoduchá interpretace • Jednonásobně nabité ionty [M+H]+; [M-H]• Analýzy komplexních směsí • Rychlá a jednoduchá příprava a analýza • Proteiny, peptidy, oligosacharidy, nukleotidy syntetické polymery ... • Tolerantní k detergentům, solím… • Krátké laserové pulsy; t ~ ns • Spojeno s TOF analyzátorem Analyzátory • q, MSQ – quadrupole (Mono Stage Quadrupole) • TSQ – Triple Stage Quadrupole (QqQ) • qIT – quadrupole Ion Trap • LT – Linear Ion Trap • Sector B/E geometry • TOF – Time Of Flight • FT-ICR – Fourier Transform – Ion Cyclotron Resonance • Hybridní (q-TOF, TOF-TOF, q-FT-ICR, LT-FT-ICR) Time Of Flight (TOF) Analyzátor Ekin = ½ mv2 Time Of Flight (TOF) Analyzátor Time Of Flight (TOF) analyzátor • Velmi vysoká transmise iontů • Teoreticky neomezený hmotnostní rozsah • Využití chlazených detektorů • Téměř současná detekce všech iontů: kompletní spektrum během každého ionizačního pulsu • Vysoké rozlišení a přesnost Post-Source Decay (PSD) Kvadrupólový analyzátor + + - + Iontová past Ionty Vyhřívaná kapilára Iontová brána Fokusační multipóly Iontová past Iontová Past • • • • Akumulace iontů Vysoká citlivost Schopnost MS/MS a MSn (MS/MS v čase) Malé rozměry • • • • Omezený dynamický rozsah Nižší rozlišení a přesnost Omezená fragmentační energie 1/3 pravidlo Trojnásobný kvadrupól N2 RF Fokusace iontů Prekursorové ionty Q1 Q2 Kolizní cela Fragmentace (CAD) Q3 Detektor Produktové ionty Q-TOF FT-ICR – Iontově cyklotronová rezonance s Fourierovou transformací Pohyb iontů v magnetickém poli - iont s hmotností m, pohybující se s rychlostí v v homogenním magnetickém poli se silou B: F = qv × B Iont pohybující se po cyklotronové orbitě s frekvencí danou vztahem: qB 2πf = m Poloměr běžné cely: 1-3 cm Počáteční poloměr pohybu iontu: 0.01 - 0.1 mm Běžná síla magnetického pole: 1-12 Tesla Pohyb iontů v magnetickém poli FTMS cela Trapping Plates, +1.0 V Detekce B Excitace + Excitace a detekce iontů r= EoTexc. 2B Signál ∝ Nions Signál ∝ r Eo Působením rezonančního dipolárního pole jsou ionty „přinuceny“ pohybovat se po cyklotronových drahách s větším poloměrem pohybu. Finální r nezávisí na m/z. Fourierova transformace (Iontově Cyklotronová Resonance) Detekce qB f = 2π m + + + + + + + + + Koherentní cyklotronový pohyb indukuje „prodový obraz“, který je amplifikován a detekován. Přítomnost iontů s různými m/z se projeví Jako superpozice sinusoidalních signálů na Detektoru. Fourierova transformace a rozlišení FT Rozlišení • Jednotkové – rozeznáme m/z 100 od 101 – kvadrupóly a iontové pasti • m/∆m – kde bereme ∆m bereme buď v 10% nebo v 50% výšky píku • Př. - rozlišení 50000 znamená, že odlišíme dvě látky, lišící se o 1/50000 MW – 1296.6775 a 1296.7034 Přesnost Absolutní • Da – Dalton - 0.1 – 0.0001 • Th – Thompson – 0.1 – 0.0001 Relativní (mění se podle m/z • ppm – parts per million – 100 – 0.1 1000.0000 • % Iontová past 100-1000 ppm TOF FT-ICR 10-100 ppm 0.1 – 1 ppm Hmotnostní spektrometrie v analýze biomolekul • Kontrola kvality/čistoty • Určení MW • Identifikace • Sekvenování • Charakterizace modifikací • Studium nekovalentních komplexů • Analýza směsí • Kvatifikace • Studium 3D struktury s nízkým rozlišením Určení MW – MALDI Určení MW – ESI R NH3+ S T R S S R NH3+ + NH3+ + NH3 R NH3 V A A R NH3+ A R NH3+ Relativní intensita G R S T G R S S R NH3+ NH3+ NH3+ R V A A R A R NH3+ S G S R S + NH3 R A A R A R R T R m/z V Určení MW – ESI Dekonvoluce… Výpočet MW proteinu z m/z sousedních píků M – MW proteinu z – nábojový stav Intensita X = (M+z)/z Y = (M+z+1)/(z+1) X Nábojový stav (z) píku X: zx= (Y-1)/(X-Y) Y MW: M = (X*zx)-zx = (Y*zy)-zy m/z Myoglobin: výpočet MW X = 998.25 Y = 942.82 zx = (Y-1)/(X-Y) = (942.82-1)/(998.25-942.82) ≈ 17 zx = 17, zy = 18 M = (X*zx) – zx = 998.25*17-17 = 16952.91 Teoretická MW = 16951.52 Neznámá molekula Í N T N A T DIS I V K E U O S )J 4 E 4 N ( ! nu ! i ! e t o ER r p M Y L vy a1101.8 O t P Xs= E é Y = 1057.8 J v o j O T bo á O n T z = (Y-1)/(X-Y) = (1057.8-1)/(1101.8-1057.8) ≈ é x n z 24 Rů zx = 24, zy = 25 M = (X*zx) – zx = 1101.8*24-24 = 26419.2 M = (Y*zy) – zy = 1057.8*25-25 = 26420 M = (662.1*34) - 34 = 22477.4 M = (1762.1*9) - 9 = 15849.9 Identifikace proteinů Protein na gelu nebo roztoku Štěpení proteinu Peptidové mapování/ Peptidový fingerprinting Identifikace proteinu - princip Proteinové štěpení • • • • • • • Trypsin Chymotrypsin AspN GluC ArgC LysC CNBr K/RY/W/K/F-D E-, E/DRKM- \-P \-P \-P \-P \-P Důležitá je přesnost… Čím vyšší přesnost měření, tím méně peptidů potřebujeme pro bezchybnou identifikaci 1000.0000 Iontová past 100-1000 ppm TOF 10-100 ppm FT-ICR 0.1 – 1 ppm □ groEL protein * ATP synthase Peptidové mapování ¾MOWSE – MRC/HGMP ¾Pro-Found – Proteometrics, Rockefeller University ¾MASCOT – Matrix Science ¾PepIdent, MultiIdent – SWISS-PROT ¾PepSEARCH – EMBL ~ PepSea – Protana ¾MS-Fit – Protein Prospector,UCSF ¾pepMAPPER – UMIST Identifikace proteinu Protein na gelu nebo v roztoku Štěpení proteinu Peptidové mapování/ Peptidový fingerprinting Bez výsledku Peptidové mikrosekvenování (PSD, MS/MS) Peptidové sekvenování Fragmentace peptidu b1 b2 b3 R1 R3 R4 R2 NH2-CH-CO-NH-CH-CO-NH-CH-CO-NH-CH-CO2H N-konec C-konec y3 y2 y1 Fragmentace peptidu S-P-A-F-D-S-I-M-A-E-T-L-K MH+ = 1410.6 b-ions+ 88.1 185.2 256.3 403.5 518.5 605.6 718.8 850.0 921.1 1050.2 1151.3 1264.4 y-ions+ S PAFDSIMAETLK SP AFDSIMAETLK SPA FDSIMAETLK SPAF DSIMAETLK SPAFD SIMAETLK SPAFDS IMAETLK SPAFDSI MAETLK SPAFDSIM AETLK SPAFDSIMA ETLK SPAFDSIMAE TLK SPAFDSIMAET LK SPAFDSIMAETL K 1323.6 1226.4 1155.4 1008.2 893.1 806.0 692.3 561.7 490.6 361.5 260.4 147.2 Další typy fragmentových iontů C-konec x3 y3 z3 R1 O H2N C H N-konec y2 R2 O C a1 x2 b1 N C H H c1 C z2 x1 y1 z1 R3 O N C H H a2 b2 c2 C a3 b3 R4 N C H H c3 COOH … a ještě další typy iontů … R1 O + R2 a2 H H R1 O R2 + H2N C C N C C O H b2 H H R1 O c2 H R2 O H + R3 O + y2 H R3 O R4 + z2 H H2N C C N C H H N-koncové: a, b, c, d C-koncové: x, y, z, v, w d2 H H O R4 H+ HN C C N C COOH H C C N C COOH H R1 O R4 H3N C C N C COOH H H2N C C N C C NH3 H R4 O C N C C N C COOH H H H H x2 H2N C C N C H R3 O + + H CHR' H v2 CHR' O C H H H R4 C N C COOH w2 H H H+ Nomenklatura fragmentových iontů peptidů Ion type Ion mass Ion type Ion mass a [N]+[M]-CO d a-partial side chain a* a-NH3 v y-complete side chain ao a-H2O w z-partial side chain a++ (a+H)/2 x [C]+[M]+CO b [N]+[M] y [C]+[M]+H2 b* b-NH3 y* y-NH3 bo b-H2O yo y-H2O b++ (b+H)/2 y++ (y+H)/2 c [N]+[M]+NH3 z [C]+[M]-NH N C M hmotnost N-koncové skupiny hmotnost C-koncové skupiny hmotnost však AK zbytků Jak spočítat hmotnost iontu? • b-ionty 1 + B1 + B2 + B3 + B4 + . . . . • y-ionty 1 + 18 + Y1 + Y2 + Y3 + Y4 + . . . . • a-ionty b – 28 (CO) • immoniové ionty AK zbytek – 27 • MW Σ(AK zbytek) + 18 Přehled aminokyselin v číslech AK G A S P V T C L I N D Q K E M H F R Y W Gly Ala Ser Pro Val Thr Cys Leu Ile Asn Asp Gln Lys Glu Met His Phe Arg Tyr Trp Hmotnost 57.02 71.08 87.03 97.05 99.07 101.05 103.01 113.08 113.08 114.04 115.03 128.06 128.09 129.04 131.04 137.06 147.07 156.10 163.06 186.08 Boční řetězec 1 15 31 41 43 45 47 57 57 58 59 72 72 73 75 81 91 100 107 130 Immoniové ionty 30 44 60 70 72 74 76 86(72) 86(72) 87(70) 88 101(84, 129) 101(129, 112, 84, 70) 102 104(61) 110(166, 138, 123, 121, 82) 120(91) 129(112, 100, 87, 73, 70, 59) 136 159 Pravidla pro čtení sekvence 1. ? Nábojový stav, hmotnost prekurzoru 2. ? C- nebo N-koncová AK – na základě štěpení 3. ? Komplementární ionty – nikdy nekombinovat různé série !!! y + b – 1 = [M+H]+ 4. ? a- / b-iontové páry (dif. 28a.m.u.) 5. ? Ztráty H2O/ NH3/ CH3SOH (dif. 18 / 17 / 64 a.m.u.) 6. ? Vícenásobně nabité ionty + následné neutrální ztráty 7. ? Prolin 1069 y8 175 y1 W S V Q I Y F E D R a1 159 • • • • • b2 274 b-ionty 1 + B1 + B2 + B3 + B4 + . . . . y-ionty 1 + 18 + Y1 + Y2 + Y3 + Y4 + . . . . a-ionty b – 28 (CO) Immoniové ionty AK zbytek – 27 MW Σ(AK zbytek) + 18 Hmotnost [M+H]+ [M+2H]2+ [M+3H]3+ [M+Na]+ 1341.6 1342.6 671.8 448.2 1364.6 m/z 699.62 tryptic digest (-K/-R) [M+H]+ = 1398.24 ends with -K AAAAAAAAAAAAAAGAAGK A A A A KG A A 6A A A A A A A A G A A G A A K A G A A A 2A A 2A [M+2H]2+ SSLPPLPGPDK y82+ y8 y7 y5 y8 y5 y7 y3 GTPGELTYSVTYTPGASTNKHPDWWNEK y15 y26 y7 y263+ [M+3H]3+ y182+ y202+ y162+ y7 y152+ y212+ y222+ y232+ y172+ y192+ y252+ y262+ Jak rozbíjet peptidy (a jiné molekuly…) • • • • • • CID – Collision Induced Dissociation CAD – Collisionally Activated Dissociation PSD – Post-Source Decay ISD/ISF – In-Source Decay/Fragmentation ECD – Electron Capture Dissociation IRMPD – Infrared Multi-Photon Dissociation • Další – EI, FAB, atd. Interpretace MS/MS Spekter ¾MASCOT MS/MS SEARCH - Matrix Science ¾MS/MS SONAR - Proteometrics, Rockefeller University ¾PepFrag – Proteometrics, Rockefeller University ¾MS Seq, MS Tag - Protein Prospector,UCSF ¾SEQUEST – Scripps, ThermoFinnigan MASCOT – MS/MS MASCOT – MS/MS výsledek Skóre Report „Error tolerant search“ report Sequence Tagging Input information: ¾short sequence (e.g.3 AA) ¾exact peptide MW ¾fragment ion type m/z1-X-Y-Z-m/z2 [M+H]+ 716.4-N-Q-Q-1086.6 [M+H]+ = 1475.7 y-ions search gi|254622| (S43646) Cytokeratin 2 …..161 VNQSLLQPLN VKVDPEIQNV KAQEREQIKT LNNKFASFID KVRFLEQQNQ VLQTKWELLQ QMNVGTRPIN LEPIFQGYID SLKRYLDGLT 250….. PepSea PROTANA Sequence Tagging ...SEARCH… Identifikace proteinů Protein na gelu nebo v roztoku Identifikace proteinu Štěpení proteinu Peptidové mapování/ Peptidový fingerprinting Bez výsledku Peptidové mikrosekvenování (PSD, MS/MS) Bez výsledku Oligonukleotidy Klonování Sekvenování DNA NEBO „de novo“ sekvenování Strategie peptidového sekvenování ¾ Zefektivnění fragmentace ¾ Preferenční tvorba jedné iontové série ¾ Odlišení iontových sérií ¾ „de novo” sekvenování ¾ Derivatizace: Chemically Assisted Fragmentation CAF ¾ H218O značení ¾ Esterifikace (EtOH: 28 Da / COOH skupinu) ¾ Ladder Sequencing Chemically Assisted Fragmentation ¾ Modifikace lysinu (guanidylace) ¾ CAF reagens (NHS-ester se sulfonovou skupinou) ¾ negativně-nabité N-koncové ionty ¾ Spektra obsahují především y-ionty ¾ Reakce: 1-2 min v 50 mM NH4HCO3/MeCN (1:1) při lab. teplotě těsně před analýzou MW = 184 Da N-konec ∆m = 184 Da Chemically Assisted Fragmentation [M+H]+ -184 Da Značení pomocí 18O Štěpení ve směsi H2O:H218O (1:1) 18OH H + trypsin 999.5 H2O 999.5 1001.5 H218O normalní H2O TQDFTDQ značaná H218O Q D T F D Q T Esterifikace » Esterifikace směsí alkohol/acetyl chlorid » modifikace Glu, Asp, C-konce » COOH skupina změněna na COOCxHy » ∆m – ethanol - 28 Da na každou COOH skupinu v peptidu Ethylesterifikace Ethylesterifikace FTQDFTDQSVK Alkylace • Cys – zlepšuje detekeci peptidů s Cys, brání tvorbě disulfidicky vázaných dipeptidů • 1.krok – redukce S-S na SH pomocí DTT, TCEP, ME. Za zvýšené teploty (65°C). • 2.krok – reakce s alkylačním činidlem. IAA, VP, AA, BrEA. Za normální teploty, v temnu a nejlépe pod dusíkem. • Při použití BrEA – Cys se mění na analog Lys – lze štěpit v daném místě pomocí Trypsinu nebo LysC. • Alkylace má význam i při kvantifikaci (ICAT, aj.) alkylace Cys během elektroforézy 2+ y20 DSLLPVSAYCDMETDGGGWTVFQR MW + 71Da ?? DSLL PVSAYCDMETDGGGWTVFQR AA „Ladder Sequencing“ ¾ ¾ ¾ ¾ ¾ ¾ z N- nebo C-konce Chemická nebo enzymatická degradace Edmanova chemie (PITC) Karboxypeptidasy (Y, P, B) Aminopeptidasy Karboxypeptidasa Y Čistý peptid Částečná oxidace methioninu – další pomoc při čtení sekvence YATFMESLR Částečná oxidace methioninu – další pomoc při čtení sekvence YATFMoxESLR Differenční proteomika – identifikace proteinů pH 3.0 250 kDa MW 10 kDa non-linear IPG pH 10.0 Proteiny ovlivněné terapií 1 Protein Spot No. 6 2 6 Protein Disulfide Isomerase P55 No. 1 & 2: Calreticulin 3 4 5 No. 3, 4 & 5: ER p57 protein No. 6: Protein Disulfide Isomerase P55 malate dehydrogenase Bottom up vs. Top down identifikace proteinů • Štěpení proteinu/směsi • MS, MS/MS (na úrovni peptidů) • LC-MS(/MS) • DTB prohledávání na bázi PMF, MS/MS • • • • • Pre-frakcionace Purifikace v plynné fázi Určení přesné MW MS/MS proteinu DTB prohledávání pomocí MW proteinu a sekvenčního „tagu“ • Zachována informace o PTM TopDown http://kelleher.scs.uiuc.edu/ Shotgun proteomics – Analýza proteinových směsí •Bez gelů - 1D nebo 2D – ztráta informace o PTM •Komplexní směsi (organely, celé buňky,…) •HPLC – 1D – RP C18 • 2D – SCX/SAX + RP C18 •3D – GF + SCX/SAX + RP C18 •2D or 3D + afinitní purifikace •data dependentní analýza •píkové parkování •“frakcionace v plynné fázi” Full MS Mass range(350-1800) Scan 1479 Full MS/MS (CID) Scan 1480 Precursor 667.7 Data-Dependent MS & Dynamic Exclusion 1 100 735.7 Relative Abundance 90 80 70 60 1469.9 2 50 40 30 490.9 20 10 0 3 971.4 5 588.5 400 500 600 700 800 903.0 900 4 1070.7 1213.7 1353.8 1500.6 1666.7 1786.0 1000 1100 1200 1300 1400 1500 1600 1700 1800 m/z 1486 - 88 AIIIFVPVPQLK (RPS7) 1478 - 80 NLQNLLILTAIK 1468 - 72 SVDPTLALSVYLR 1470 SVNESLNNLFITEEDYQALR 1450 - 52 TTGFGMIYDSLDYAK (RPS24) 1418 - 20 LLEPVLLLGK (RPS16) 1414 - 22 TDITYPAGFM*DVISIDK (RPS4) 1412 LTDQLPLIIVCDR 1410 WLLLTGISAQQNR „Gas-phase Fractionation“ 100 Relative Abundance 90 1 735.7 1 2 3 80 70 1 60 1469.9 50 40 2 30 20 10 0 1 490.9 2 588.5 400 500 2 971.4 600 700 800 903.0 900 1070.7 1213.7 1353.8 1500.6 1666.7 1786.0 1000 1100 1200 1300 1400 1500 1600 1700 1800 m/z Kvatifikace pomocí MS • ESI, (MALDI) • Interní standart – stejné podmínky ionizace • Izotopické značení – ICAT – Isotope Coded Affinity Tags – značí jen některé AK, zjednodušuje komplexitu směsi, izotopický efekt H/D – PhIAT – Phosphoprotein Isotope Coded Affinity Tags – kvantifikace Pproteinů – D3/H3 acrylamid – značí jen Cys, nezjednodušuje komplexitu, menší izotopický efekt – D3/H3 esterifikace – značí C-konec, D, E, nezjednodušuje komplexitu, malý izotopický efekt – SILAC – Stable Isotope Labelling – přídavek L/I (C12/13, N14/15), žádný izotopický efekt, mnoho různých peptidů je značeno, komplexita směsi zůstává – AQUA – Absolute Quantification of Abundance Isotope Coded Affinity Tag (ICAT) reagens O N XX O N S Biotin tag XX O XX O O O XX N Linker (těžký nebo lehký) I Thiol reaktivní skupina 100 Relative Magnitude N d0- or d8-ICAT (X= H nebo D) LDQWLCEK d0 d8 1520 1525 50 0 800 1200 m/z 1600 1530 1535 1540 2000 2400 Kvatifikace a identifikace pomocí ICAT ICAT-em značené cysteiny Směs 2 y n ra ra l b o s m jád o e t y m c Případná frakcionace Směs 1 100 Light 0 550 100 Smíchat a štěpit 560 Heavy 570 m/z 580 NH2-EACDPLR-COOH Afinitní separace 0 200 400 600 m/z 800 Kvantifikace a identifikace proteinů ICAT vs . in vitro značení Stav 1 SILAC in vivo značení Stav 2 znační Sklízení buněk Stav 1 Sklízení buněk Stav 2 značení Stav 2 Stav 1 1+2 Smíchání buněk Přečištění 1+2 Smíchání proteinů Přečištění Štěpení trypsinem a analýza LC-MS/MS Štěpení trypsin a Analýza LC-MS/MS AQUA Absolute Quantification of Abundance Gerber SA, PNAS 2003, 100:6940 Nutná znalost toho, co známe. Peptid vytipován na základě předchozích pokusů Vhodné pro “lovení” málo abundantních proteinů (SRM mode) Výběr vhodného peptidu: Ne M, W, H Ne KK, KR, RR nebo i KXR, KXK, KXXK Vhodná velikost – Nábojový stav Funkční proteomika – Analýza komplexů aneb kdo s kým.. Nativní elektroforéza S40 Ribosome subunit kDa 667 Proteasome S26 440 230 Clathrin ATP synth. F1 140 67 MARKER Calreticulin RNK16 KIDNEY Monitorování místa zásahu enzymu gliadin fragment VSFQQPQQQYPSSQ tTG enzym Q ⇔ E ∆1 Da 0 min VSFQQPQQEYPSSQ + 30 min VSFEQPQQEYPSSQ + ++ 3 hrs PostTranslační Modifikace • Disulfidické můstky (CysCys) • Glykosylace • Fosforylace • Acylace • • • • • Oxidace Acetylace Zkrácení Ztráta N-konc.Met Glu -> pyro-Glu Disulfidické můstky A - určení zda jsou nebo nejsou přítomné – diferenční alkylace B – určení kolik Cys je volných a kolik vázaných 1. denaturace, alkylace činidlem I (u menších proteinů lze rovnou měřit MS) 2. redukce a alkylace činidlem II 3. štěpení a MS, LC-MS/MS – určení C – přímá identifikace disulfidů - štěpení + LC-MS (FTICR) – hledání disulfidicky spojených peptidů podle přesné hmotnosti D – izolace disulfidicky spojených peptidů a jejich identifikace MS popřípadě Edman. oddouráváním Diferenční alkylace – celý protein Disulfidické můstky štěpnení pepsinem nebo chymotrypsinem ½ redukována, ½ nativní diferenční HPLC (RP, IXC) – vytipování frakcí MS analýza, +/- redukční činidlo MS/MS pro určení sekvence peptidů Disulfidické můstky + DTT redukce S-S vazby Disulfidické můstky PSD Disulfidické můstky Disulfidické můstky Y L D C G H G G F N Y G G N G G S W C A P Y K T M1 + M2 +H+ - 2H (z Cys) = [M1-S-S-M2+H]+ (967.4 + 1573.7) + 1 - 2 = 2540.1 Glykosylace • Mnoho důležitých funkcí: stabilizace struktury, dobré poskládání, ochrana před degradací, interakce ligandreceptor, targeting, modulace aktivity • N-glykosylace na sekvenci: NXT/S/C – v β-strukturách nebo smyčkách sacharid: větvený, 3 typy: mannosový, komplexní, hybridní • O-glykosylace nemá klasický motiv S, T, ale také hydroxyPro, Lys, atd. sacharid: cokoliv od monosacharidu pro dlouhé, případně mírně větvené struktury N-glykosylace • Určení zda protein je nebo není glykosylován a - podle mobility na gelu+deglykosylace b - lektin-blot – určuje terminální sacharidy c - přímo v MS d - glykoproteinové barvení b) a) TMSF PNGase F c) 1 2 3 4 5 6 – – – – – – ConA LCA PNA SBA WGA UEA d) • • • Oxidace kys. Jodistou Přidání Schiffova reagens (kys. fuchsinsiřičitá) Odbarvení pozadí Alternativy s fluorescencí nebo biotinylací Použitelné i pro histologii N-glykosylace 1. 2. 3. 1. 2. 3. Charakterizace sacharidových struktur+určení heterogenity Nalezení míst glykosylace Přiřazení struktur na jednotlivá glykosylační místa a) uvolnění glykanu(-ů) – enzymaticky – PNGasa F, Endo H, Endo F1-3, postupné odštěpování pomocí exoglykosidas, Pronasa chemicky – hydrazinolýza, alkalické štěpení, TMSF – (pouze deglykosyluje – ničí sacharid) b) charakterizace glykanů – NMR, MS, MS/MS, permethylace+MS/MS, exoglykosidasy+MS a) Edmanovo odbourávání – nejlépe glykopeptidy peptidy po EndoH b) deglykosylace PNGasouF v H216O a H218O (+ štěpení AspN) – PNGasa F mění Asn na Asp (vzniká zásahové místo pro AspN) Štěpení proteinu – izolace glykopeptidů a opakovaní postupu na jednotlivých glykopeptidech Glycan MS/MS – nomenclature Domon-Costello (1998) Glycosylation: PSD-MALDI MS Deglykosylace PNGasouF v H216O a H218O Asn -> Asp 16O -> 18O +1 a.m.u. +2 a.m.u. Posun proti hmotnosti původní sekvence + 3 a.m.u. Jak to lze urychlit? - přímá analýza glykopeptidů • Štěpení různými proteázami a LC-MS/MS (iontová past, q-tof, q-FT-ICR) nebo LC-MS (FT-ICR) • Jak identifikovat glykopeptidy a) hledáme v MS záznamu diference odpovídající sacharidům (např. 162, 81, 54 pro Hexosu) b) použijeme speciální nastavení a pomocí ISF generujeme charakteristické ionty v oblasti malých m/z (163, 204, 274, 292, 366) c) pomocí SW hledáme glykopeptidy podle velice přesných m/z (FT-ICR) Glycopeptide: ESI MS/MS (nejenom) Peptidové sekvenování ve FTMS Infrared Multiphoton Dissociation (IRMPD) • CO2 laserový paprsek • Vibrační excitace funkčních skupin OH, COOH, NH2… • Fragmentace peptidové páteře: b- a y-iontové series • Určení / ověření sekvence • Za mírnějších podmínek pouze ztráta labilních skupin - PTM (nejenom) Peptidové sekvenování ve FTMS Electron Capture Dissociation (ECD) • Záchyt „studeného“ elektronu (E ≤ 0.1 eV) preferenčně na S-S můstcích a vazbě N-Cα • Neutralizace H+; [M+2H]+. Vodíkem nabohacený radikálový iont • Štěpení vazby N-Cα; extensivní fragmentace • c- a z-iontové série; b- a y-ionty chybí • Prefenční štěpení peptidové vazby, jsou zachovány labilní skupiny modifikací • „Horké“ ECD (3-13 eV); sekundární fragmentace – z ionty tvoří ionty w ECD Glykopeptidu Anal. Chem. 2001, 73; 4530 ECD Glykopeptidu Anal. Chem. 2001, 73; 4530 IRMPD Glykopeptidu Anal. Chem. 2001, 73; 4530 IRMPD Glykopeptidu Anal. Chem. 2001, 73; 4530 IRMPD Glykopeptidu Anal. Chem. 2001, 73; 4530 IRMPD Glykopeptidu Anal. Chem. 2001, 73; 4530 Kombinace IRMPD & ECD • Komplementární techniky pro řešení peptidové/proteinové sekvence a lokalizaci a identifikaci PTMs • Může být provedeno během jednoho experimentu • Analýza glykopeptidů, fosfopeptidů, lokalizace γkarboxyglutamové kys., rozlišení Ile/Leu… Fosforylace Signalizace, aktivace,… S, T, Y, H Ztráta (P) skupiny: -98, -80 - Směrovaná MS analýza (neutrální ztráta, precursor ion scanning, negativní mód) Nabohacení – protilátky, IMAC Působení fosfatázy / alkalií + diferenční mapování „Vychytávání“ fosfopeptidů: eliminace, adice afinitní skupiny 2D P-peptidové mapování (elektroforéza/TLC) Fosforylace A 4 3 .3 0 100 90 3 2 .8 2 Relative Abundance 80 70 60 3 7 .3 5 50 40 2 6 .6 5 30 2 8 .0 1 3 5 .9 3 3 0 .0 3 20 4 2 .4 2 3 9 .3 1 10 3 4 .1 1 2 8 .9 8 4 4 .3 3 4 1 .1 3 0 B 2 9 .9 6 100 90 49 Da neutrální ztráta Relative Abundance 80 Možné fosfopeptidy 70 60 50 40 30 2 6 .1 2 20 3 5 .9 1 10 0 2 7 .7 1 2 4 .9 0 25 26 27 28 29 3 2 .9 0 3 1 .0 1 2 8 .8 6 30 31 32 33 3 4 .2 7 34 35 3 7 .3 8 36 T im e (m in) 37 38 3 9 .0 9 4 0 .3 34 1 .2 6 39 40 41 4 2 .4 5 42 43 4 3 .8 7 4 4 .9 4 44 45 Fosforylace GVVTNGLDLSPADEK * Loss Ztráta of phosphate fosfátu (m/z749) (m/z749) Parent Rodičovský ion position iont (m/z (m/z798) 798) IMAC – Immobilized Metal Ion Affinity Chromatography • IDA (iminodiacetic acid) NTA (nitrilo-triacetic acid) • Iont kovu – Ga3+, Fe3+ • Nespecifická vazba – esterifikace Působení alkalického prostředí P-peptidy P-peptidy po působení alkálií Mol. Cell. Proteom. 2002, 1:186-196 “vychytání” fosfopeptidů •Oxidace Cys •Eliminace •Adice ethanedithiolu •Biotinylace •Afinitní purifikace •MS, MS/MS •POUZE PRO pS, pT !!! Nat. Biotech. 2001, 19:379-382 Flavoprotein – lokalizace flavinu? RP-HPLC tryptického/chymotryptického digestu 220 nm 450 nm flavopeptid Flavoprotein – lokalizace flavinu? MALDI-MS intaktního (?) flavopetidu PSD [M+H]+ Flavoprotein – lokalizace flavinu? PSD MALDI-MS H a3-NH3-H2O a3-NH3 b3-H2O S-T-H-W [M+H]+ b3 y2 H W S T y1 a2 b2 a4 a3 y3 b4 Flavoprotein – lokalizace flavinu? MALDI-MS intaktního (?) flavopetidu PSD [M+H]+ [f+2H]+ 348 [j+2H]+ 136 h+ 250 438 Struktura flavopeptidu 785 [d+2H]+ 428 O H N O HN 4 N 4a 5a 6 2 O 7 CH3 ? 9 N 10a 1 N 8 9a CH3 H OH H OH CH2 5 HN 1 NH2 f O 6 N O O P O P O HO 438 d His N 3 2 OH Thr 4 CH2 H 5 Trp OH 2 CH2 5 HO h N 5 4 O 4 3 N N 8 1 2 OH j Ser QDPTDVGEAFANVEWSVAELKR 2461.2 did not fit + 17Da bigger Gln O NH2 C C H2 C H2 O H C C NH2 N H R (111)D PTDVGEAFANVEWSVAELKR NH3 H2C H C H2C NH O C N H C O pyro-Glu R 128-17=111 pyro-Glu !!! Určování 3D struktur pomocí FT-ICR MS – MS3D - proteiny jejichž str. není řešitelná krystalografií nebo NMR (MW > 30kDa, flexibilní domény, membránové proteiny, proteiny s PTMs,…) - Surface accessibility – povrchové značení a reaktivita AK – jedna reaktivní skupina O N O C CH3 O O - Intramolekulární zesíťovací činidla (cross-linkers) – dvě a více reaktivních skupin, odděleny raménkem o různé délce – tzv. molekulární pravítka O O O N O O C 11.4 Å DSS O N O O O O C N O O O O O C O C 7.5 Å DSG O N O N O O OH O C C OH O 5.8 Å DST O N O
Podobné dokumenty
Investigation of NKR-P1 Membrane-Protein Complex by MALDI
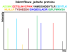 • pY [MH-80]+, pS,pT [MH-98]+
• Neutrální ztráta (pS, pT: 98, 49, 33)
• P-peptidy spouštěné MS3 (MS2 – je-li ztráta P -> MS3
• pY [MH-80]+, pS,pT [MH-98]+
• Neutrální ztráta (pS, pT: 98, 49, 33)
• P-peptidy spouštěné MS3 (MS2 – je-li ztráta P -> MS3
MUTACE A JEJICH KLINICKÉ DOPADY
 DEFEKTY KARDIOVASKULÁRNÍHO SYSTÉMU
http://www.icomm.ca/geneinfo/wolf.htm
DEFEKTY KARDIOVASKULÁRNÍHO SYSTÉMU
http://www.icomm.ca/geneinfo/wolf.htm
âESKÁ SPOLEâNOST PRO BIOCHEMII A MOLEKULÁRNÍ
 Po úspěšné identifikaci bílkoviny jsou experimentální molekulové hmotnosti peptidů
přiřazeny k sekvencím peptidů a tím je určena primární struktura analyzovaných peptidů. V dalším textu se pod pojm...
Po úspěšné identifikaci bílkoviny jsou experimentální molekulové hmotnosti peptidů
přiřazeny k sekvencím peptidů a tím je určena primární struktura analyzovaných peptidů. V dalším textu se pod pojm...
Lysosomální enzymopathie: dědičné poruchy funkcí lysosomů
 Snížená aktivita enzymu u klinicky zdravých jedinců:
kromě ASA existuje i u mutací dalších lysosomálních hydrolas
Snížená aktivita enzymu u klinicky zdravých jedinců:
kromě ASA existuje i u mutací dalších lysosomálních hydrolas
rr3oNgsny"z - Spiritismus
 ::li"T#+lĚggE;íEŤra H.ř* $; řr:gHln*Eaiii
;t = E : 0 - = ' T a ! 3- ' r B , d = f t
i=i 1gí;
::li"T#+lĚggE;íEŤra H.ř* $; řr:gHln*Eaiii
;t = E : 0 - = ' T a ! 3- ' r B , d = f t
i=i 1gí;
studie mcl elderly
 - pacient může být podruhé randomizován, jen když dosáhl KR, uKR, PR
Vyřazující kriteria
- PS 3 a více
- není-li CD20+
- leukocyty pod 2x109/l a/nebo trombocyty pod 100 x 109/l, není-li infiltrovan...
- pacient může být podruhé randomizován, jen když dosáhl KR, uKR, PR
Vyřazující kriteria
- PS 3 a více
- není-li CD20+
- leukocyty pod 2x109/l a/nebo trombocyty pod 100 x 109/l, není-li infiltrovan...
Analýza těkavých látek
 m2.g-1, objemem pórů 2,4 cm3.g-1, průměrnou velikostí pórů 200nm
a hustotou 0,25 g.cm-3, jeho teplotní stabilita je uváděna až do
350°C. Díky uvedeným vlastnostem, nízkému obsahu nečistot a
dobré s...
m2.g-1, objemem pórů 2,4 cm3.g-1, průměrnou velikostí pórů 200nm
a hustotou 0,25 g.cm-3, jeho teplotní stabilita je uváděna až do
350°C. Díky uvedeným vlastnostem, nízkému obsahu nečistot a
dobré s...
Bioprospect - Biotechnologická společnost
 protilátka tvořená B‑lymfocyty vznikajícími v kostní dřeni. Tyto poznatky se staly návodem k vývoji léčiv vhodných k léčbě Alzheimerovy choroby. Jedná se o léky
schopné bránit formě plaku nebo/a j...
protilátka tvořená B‑lymfocyty vznikajícími v kostní dřeni. Tyto poznatky se staly návodem k vývoji léčiv vhodných k léčbě Alzheimerovy choroby. Jedná se o léky
schopné bránit formě plaku nebo/a j...
 rozdílná velikost má vliv na migraci
rozdílná velikost má vliv na migraci
 Seminář VI CESNET, Seč, 3. dubna 2012
Seminář VI CESNET, Seč, 3. dubna 2012





