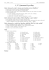Write the following stoichiometric chemical equations in ionic form
Transkript
Medical Chemistry, First Year General Medicine 2005/2006 PRACTICE Write the following stoichiometric chemical equations in ionic form AgNO3(aq) + AgCl(s) HCl(aq) ⎯→ AgCl(s) + + 2 NH4OH(aq) ⎯→ 2 AgNO3(aq) + HNO3(aq) [Ag(NH3)2]Cl(aq) + 2 H2O(l) ⎯→ Ag2CrO4(s) + 2 KNO3(aq) K2CrO4(aq) Pb(NO3)2(aq) + 2 HCl(aq) ⎯→ PbCl2(s) + 2 HNO3(aq) Pb(NO3)2(aq) + H2S(aq) ⎯→ PbS(s) + 2 HNO3(aq) 2 HgNO3(aq) + 2 HCl(aq) ⎯→ Hg2Cl2(s) + 2 HNO3(aq) CuSO4(aq) + Cu(OH)2(s) + Na2SO4(aq) ⎯→ [Cu(NH3)4]SO4(aq) + 4 H2O(l) CuSO4(aq) + 4 NH4OH(aq) Hg(NO3)2(aq) + ⎯→ 2 NaOH(aq) H2S(aq) ⎯→ HgS(s) + 2 HNO3(aq) Hg(NO3)2(aq) + 2 KI(aq) ⎯→ HgI2(s) + 2 KNO3(aq) HgCl2(aq) + 2 NH4OH(aq) ⎯→ Hg(NH2)Cl(s) + NH4Cl(aq) + 2 H2O(l) 4 FeCl3(aq) + 3 K4[Fe(CN)6](aq) ⎯→ Fe4[Fe(CN)6]3(s) + 12 KCl(aq) FeCl3(aq) + KSCN(aq) ⎯→ [Fe(H2O)5SCN]Cl2(aq) CaCl2(aq) + Na2CO3(aq) ⎯→ CaCO3(s) + 2 NaCl(aq) Ba(NO3)2(aq) + H2SO4(aq) + KCl(aq) ⎯→ BaSO4(s) + 2 HNO3(aq) Na2CO3(s) + 2 HCl(aq) ⎯→ CO2(g) + 2 NaCl(aq) + H2O(l) H2SO4(aq) + 2 KOH(aq) ⎯→ K2SO4(aq) + 2 H2O(l) Ba(OH)2(aq) + 2 CH3COOH(aq) ⎯→ Ba(CH3COO)2(aq) + H2O(l) Zn(s) + 2 HCl (aq) ⎯→ ZnCl2(aq) + H2(g) NH4Cl(aq) + NaOH(aq) ⎯→ NaCl(aq) + NH3(g) + H2O(l) 2 CuSO4(aq) + K4[Fe(CN)6](aq) ⎯→ Cu2[Fe(CN)6](s) + 2 K2SO4(aq) BiCl3(aq) + 3 NaOH(aq) ⎯→ Bi(OH)3(s) + 3 NaCl Na3AsO3(aq) + 3 AgNO3(aq) ⎯→ Ag3AsO3(s) + 3 NaNO3(aq) MgCl2(aq) + Na2HPO4(aq) + NH4OH(aq) + NH4Cl(aq) ⎯→ NH4 MgPO4(s) + 2 NaCl(aq) + H2O(l) + NH4Cl(aq) © Institute of Medical Biochemistry, 1st Faculty of Medicine, Charles University in Prague, 2005
Podobné dokumenty
05._Dukaz aniontu
 KVALITATIVNÍ ANALÝZA ANIONTŮ
Cíle a princip:
Prokázat přítomnost aniontů ve vzorku pomocí charakteristických reakcí se
specifickými činidly.
KVALITATIVNÍ ANALÝZA ANIONTŮ
Cíle a princip:
Prokázat přítomnost aniontů ve vzorku pomocí charakteristických reakcí se
specifickými činidly.
Redox rovnice
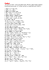 1. HgS + O2 –> Hg + SO2
2. 2BaO + O2 –> 2BaO2
3. 2PbS + 3O2 –> 2PbO +2SO2
4. 4HI + 1H2SO4 –>2 I2 + H2S + 4H2O
5. 2BiCl3 + 3SnCl2 –> 2Bi + 3SnCl4
6 . 2 HgCl2 + SnCl2 –> Hg2Cl2 + SnCl4
7. Hg2Cl2 + Sn...
1. HgS + O2 –> Hg + SO2
2. 2BaO + O2 –> 2BaO2
3. 2PbS + 3O2 –> 2PbO +2SO2
4. 4HI + 1H2SO4 –>2 I2 + H2S + 4H2O
5. 2BiCl3 + 3SnCl2 –> 2Bi + 3SnCl4
6 . 2 HgCl2 + SnCl2 –> Hg2Cl2 + SnCl4
7. Hg2Cl2 + Sn...
Úpravy chemických rovnic – procvičování (kvinta + 1.G)
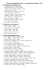 24. 6 KI + K2Cr2O7 + 4 H2SO4
3 I2 + Cr2(SO4)3 + 4 K2SO4 + 7 H2O
25. 4 NH3 + 5 O2
4 NO + 6 H2O
26. I2 + 5 Cl2 + 6 H2O
2 HIO3 + 10 HCl
27. AsH3 + 8 HNO3
H3AsO4 + 8 NO2 + 4 H2O
28. Cr2O3 + 3 KNO3 + 2 ...
24. 6 KI + K2Cr2O7 + 4 H2SO4
3 I2 + Cr2(SO4)3 + 4 K2SO4 + 7 H2O
25. 4 NH3 + 5 O2
4 NO + 6 H2O
26. I2 + 5 Cl2 + 6 H2O
2 HIO3 + 10 HCl
27. AsH3 + 8 HNO3
H3AsO4 + 8 NO2 + 4 H2O
28. Cr2O3 + 3 KNO3 + 2 ...
Pracovní list řešení
 4. Ze zinku je třeba připravit sulfid zinečnatý o hmotnosti 2,5g. Zjistěte hmotnost potřebného zinku.
1,68g Zn
4. Ze zinku je třeba připravit sulfid zinečnatý o hmotnosti 2,5g. Zjistěte hmotnost potřebného zinku.
1,68g Zn
PL - VYČÍSLOVÁNÍ ROVNIC
 Pracovní list:
Vyčísli rovnice:
HgO → Hg + O2
S + O2 → SO2
C + O2 → CO2
Ca + O2 → CaO
Fe + 3 O2 → Fe2O3
Cu + O2 → CuO
H2 + Cl2 → HCl
Na + HCl → H2 + NaCl
Zn + HCl → ZnCl2 + H2
CuO + HCl → H2O + CuCl2
Pracovní list:
Vyčísli rovnice:
HgO → Hg + O2
S + O2 → SO2
C + O2 → CO2
Ca + O2 → CaO
Fe + 3 O2 → Fe2O3
Cu + O2 → CuO
H2 + Cl2 → HCl
Na + HCl → H2 + NaCl
Zn + HCl → ZnCl2 + H2
CuO + HCl → H2O + CuCl2
Názvosloví anorganických sloučenin – pracovní list – řešení:
 Názvosloví anorganických sloučenin – pracovní list – řešení:
1) Vytvořte název solí:
Názvosloví anorganických sloučenin – pracovní list – řešení:
1) Vytvořte název solí:

 Selektivní reakce:
b) Alkalické chromany
Na2CrO4 , K2CrO4
Selektivní reakce:
b) Alkalické chromany
Na2CrO4 , K2CrO4
 Látka
Látka
 3. Napište vztah pro výpočet rovnovážné konstanty těchto reakcí:
3. Napište vztah pro výpočet rovnovážné konstanty těchto reakcí: