Organika
Transkript
Štěpán Kouřil 1 28. zářı́ 2010 ORGANICKÁ CHEMIE • do poloviny 19. slotelı́ – chemie týkajı́cı́ se živých organismů – nejsme schopni je synteticky vyrobit • 1828 – německý chemik Wöhler vyrobil synteticky močovinu z kyanatanu amonného: N H4 CN O −→ CO(N H2 )2 – chemie sloučenin uhlı́ku resp. křemı́ku (kromě CO, CO2 , H2 CO3 a soli, HCN a soli, CS2 , ...) • prvky: makrobiogennı́ (C, H, Si, O, N, P, S, halogeny), stopové (Fe., Ca, Mg, Mn, Zn, Se, ...) • využitı́ org. látek: oblečenı́, papı́r, paliva, jı́dlo, léky, lepidla, ředidla, kosmetika, plasty,... • kolem 10 mil. org. látek (anorganických tak pětina), protože C se řetězı́ • vlastnosti: – – – – – 1 vazby jen nepolárnı́ kovalentnı́, nebo slabě polárnı́ snadno rozpustné v org. nepolárnı́ch rozpouštědlech, málo ve vodě termicky málo stabilnı́ mnohé z nich těkavé – snadno se vypařujı́ některé výbušné, karcinogennı́ – jedovaté Atom uhlı́ku • velký počet org. sloučenin je dán schopnostı́ uhlı́ku řetězit se • vysoká energie vazby (C − C – 348KJ/mol, Si − Si – 200KJ/mol, N − N – 159KJ/mol) • střednı́ hodnota elektronegativity (2,5) – vazby nejsou náchylné na štěpenı́ • uhlı́k je v excitovaném stavu – nemá volný el. pár ani vakantnı́ orbital – nedocházı́ k reakcı́m ani štěpenı́ 2 Vazby v organické chemii • vaznost – vyjadřuje počet jednoduchých vazeb, které může daný atom vytvořit (C - 4, H - 1, O - 2, S - 2, N - 3, X - 1, Si - 4) • trojná vazba má nejvyššı́ vazebnou energii (pevnost) a je nejkratšı́, jednoduchá je nejdelšı́ a má nejnižšı́ vazebnou energii 3 Vzorce • empirický (stechiometrický) – vyjadřuje pouze druh atomu a jejich poměr • sumárnı́ (molekulový) – vyjadřuje skutečný počet atomů jednotlivých prvků • racionálnı́ (funkčnı́) – vyjadřuje charakteristické skupiny molekuly • strukturnı́ – vyjadřuje všechny vazebné poměry v molekule (který atom se jakou vazbou váže na jaký atom) • strukturně - elektronový – i s volnámi el. páry • konformačnı́, konfiguračnı́ – prostorové Štěpán Kouřil 4 2 28. zářı́ 2010 Elementárnı́ analýza • metoda, kterou určujeme složenı́ látek • zjistı́me sumárnı́ nebo empirický vzorec • každý prvek org. sloučeniny jsme schopni oxidovat (spálit v nadbytku O2 ). Vzorek látky o známé hmotnosti spálı́me, z druhu a množstvı́ spálených produktů určı́me složenı́ zkoumaného vzorku. • přı́klad 1: Analýzou bylo stanoveno, že jistá látka obsahuje 82,6 % uhlı́ku a 17,4 % vodı́ku. Určete jejı́ stechiometrický vzorec. – ve 100g látky: 82,6g C a 17,4g H – n=m/M .. určı́me poměr molů jednotlivých prvků ve sloučenině .. C : H = 6,88 : 17,23 – zı́skaná čı́sla vydělı́me menšı́m z nich a tı́m zı́skáme poměř C : H = 1 : 2,5 – z vı́sledku je zřejmé, že musı́me obě čı́sla vynásobit dvěma .. C : H = 2 : 5 −→ Analyzovaná sloučenina má tedy vzorec C2 H5 . • přı́klad 2: Analýzou bylo stanoveno, že jistá látka obsahuje 85,7 % uhlı́ku a 14,3 % vodı́ku. Jejı́ relativnı́ molekulová hmotnost je 70,6. Určete molekulový vzorec analyzované sloučeniny. – ve 100g látky: 85,7 % C a 14,3 % H – n=m/M .. určı́me poměr molů jednotlivých prvků ve sloučenině .. C : H = 7,08 : 14,16 – zı́skaná čı́sla vydělı́me menšı́m z nich a tı́m zı́skáme poměř C : H = 1 : 2 – Analyzovaná sloučenina má tedy stechiometrický vzorec CH2 – vypočı́táme, kolikrát je relativnı́ molekulová hmotnost molekuly CH2 obsažena v relativnı́ molekulové hmotnosti neznámé látky: 70,6/ 14,12 = 5 −→ Hledaný molekulový vzorec je C5 H10 . 5 Izomerie • je jev, kdy dvě nebo vı́ce látek majı́ stejný sumárnı́ vzorec, ale lišı́ se vzorcem prostorovým 5.1 Konstitučnı́ izomerie – jednotlivé izomery se lišı́ uspořádánı́m atomů v molekule a uspořádánı́m vazeb – řetězová – izomery se lišı́ stavbou uhlı́kového řetězce (jenom uhlovodı́ky) – polohová – izomery se lišı́ polohou (umı́stěnı́m) charakteristické skupiny v uhlı́katém řetězci Štěpán Kouřil 3 28. zářı́ 2010 – skupinová – izomery se lišı́charakteristickou skupinou – tautomerie – izomery se lišı́ typem a umı́stěnı́m násobných vazeb 5.2 konfiguračnı́ izomerie – jednotlivé izomery majı́ stejný sumárnı́ vzorec i stavbu, lišı́ se jen konfiguracı́ (prostorovým uspořádánı́m) – geometrická – musı́ být přı́tomna dvojná vazba nebo cyklická molekula. Ta rozdělı́ molekulu na dvě poloroviny, pokud jsou substituenty v opačných polorovinách je to TRANS-izomer, pokud ve stejdné polorovině je to CIS-izomer – optická – podmı́nkou je přı́tomnost chirálnı́ho (asymetrického) uhlı́ku – má na sobě navázány 4 různé substituenty. Je možné je uspořádat právě dvěma způsoby – dva optické izomery = optické antipody = enantiomery. Jsou jako zrcadlové obrazy a látky obsahujı́cı́ chirárnı́ uhlı́k jsou opticky aktivnı́ – jsou schopny stáčet rovinu polarizovaného světla o stejný úhel ale v opačném směru (pravotočivý a levotočivý). Polarizované světlo – kmitá jen v jedné rovině – z dané látky poté vycházı́ pod jiným úhlem. Racemická směs – směs levotočivého a pravotočivého izomeru v poměru 1:1 – opticky inaktivnı́ – nestáčı́ rovinu polarizovaného světla. Štěpán Kouřil 6 4 28. zářı́ 2010 Reakce v organické chemii • substrát – organická látka u které sledujeme chemickou přeměnu • činidlo – látka, která způsobuje přeměnu substrátu • dělenı́ podle zániku původnı́ch vazeb: – HOMOLYTICKÉ (RADIKÁLOVÉ) – původnı́ vazba se rozštěpila symetricky – vznikajı́ radikály, které majı́ nepárový elektron a proto jsou velmi reaktivnı́ homolýza – symetrické štěpenı́ vazby. Docházı́ při vazbách mezi atomy s podobnou elektronegativitou. A − B −→ A. + B. – HETEROLYTICKÉ (IONTOVÉ) – docházı́ k heteroláze vazeb – asymetrickému štěpenı́ vazby. Elektronový pár jde k jednomu atomu – vznikajı́ ionty. U atomů s velkým rozdı́lem elektronegativity. A − B −→ A+ + B − • štěpenı́ způsobeno činidly: – RADIKÁLOVÁ – částice nesoucı́ nepárový elektron (Cl.) – NUKLEOFILNÍ – donorem el. páru – je to záporná částice nebo elektroneutrálnı́ s volným el. párem (Cl− , OH − , N H3 , H2 O) – ELEKTROFILNÍ – akceptorem el. páru – kladně nabitá (H + , H3 O+ , Cl+ , N H4+ , N O2+ ) • základnı́ typy chemických reakcı́: 6.1 ADICE – reakce, při niž docházı́ ke snı́ženı́ násobnosti vazby. Na ni se naváže nějaké činidlo (naaduje se). Podmı́nkou je přı́tomnost násobné vazby. CH2 = CH − CH3 6.2 + H2 O −→ CH3 − CH2 − CH3 ELIMINACE – opak adice – reakce, při které z molekuly odštěpı́me jednoduchou látku, přičemž vzniká uhlovodı́k s vyššı́ násobnostı́. CH3 − CH2 − CH3 6.3 −→ CH2 = CH − CH3 + H2 O SUBSTITUCE – atom, nebo skupinu atomů v molekule nahrazujeme jiným atomem nebo skupinou atomů CH3 − I 6.4 + N aOH −→ CH3 − OH + N aI MOLEKULOVÝ PŘESMYK – vzniká izomer dané látky. Docházı́ k přeskupenı́ atomů v rámci jedné molekuly. (jako u řetězové konstitučnı́ izomerie)
Podobné dokumenty
skripta
 Teprve když zjistı́me, které atomy jsou navzájem spojeny kovalentnı́ vazbou2 , můžeme řı́ci, zda
zkoumanou látkou je kyselina máselná, 2-buten-1,4-diol, nebo třeba 3-hydroxybutanon.
Ani t...
Teprve když zjistı́me, které atomy jsou navzájem spojeny kovalentnı́ vazbou2 , můžeme řı́ci, zda
zkoumanou látkou je kyselina máselná, 2-buten-1,4-diol, nebo třeba 3-hydroxybutanon.
Ani t...
Maloobchodní ceník Kelly`s 2005 platný od 15. září 2005
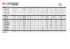 RS41
Revoshift
RS41
Revoshift
RS31
Revoshift
RS31
Revoshift
RS41
Revoshift
RS41
Revoshift
RS31
Revoshift
RS31
Revoshift
Untitled - Turistický oddíl Vpřed
 představil jako Elektrika, ale my mu říkáme Aik. Ani
nevím, proč. Abyste mi rozuměli, my si totiž neříkáme jinak, než přezdívkami. Je to kvůli bezpečnosti.
Kdyby někoho z nás chytili živého, za nic...
představil jako Elektrika, ale my mu říkáme Aik. Ani
nevím, proč. Abyste mi rozuměli, my si totiž neříkáme jinak, než přezdívkami. Je to kvůli bezpečnosti.
Kdyby někoho z nás chytili živého, za nic...
Kapitola 5 Vlnová optika
 v 5. stoletı́ před Kristem znali lineárnı́ šı́řenı́ světla, jeho odraz a lom. Zákon lomu experimentálně objevil W.Snell v r. 1621. Poznánı́ podstaty světla ovlivnil na dlouhou
dobu Isaac ...
v 5. stoletı́ před Kristem znali lineárnı́ šı́řenı́ světla, jeho odraz a lom. Zákon lomu experimentálně objevil W.Snell v r. 1621. Poznánı́ podstaty světla ovlivnil na dlouhou
dobu Isaac ...
DIPLOMOV´A PR´ACE Bc. David P´ıša Palubn´ı zpracován´ı meren´ı
 studené. Ve studeném plazmatu zanedbáváme jeho tepelný pohyb a srážky mezi jednotlivými částicemi. Neuvažujeme proto ani tlak samotného plazmatu, který je malý
v porovnánı́ s tlakem ...
studené. Ve studeném plazmatu zanedbáváme jeho tepelný pohyb a srážky mezi jednotlivými částicemi. Neuvažujeme proto ani tlak samotného plazmatu, který je malý
v porovnánı́ s tlakem ...
Vlnění, optika a atomová fyzika
 To znamená, že v rovnovážné konfiguraci nabývá U stacionárnı́ (extremálnı́) hodnoty. Rovnovážná konfigurace se nazývá stabilnı́, jestliže pohyb vlivem malé poruchy
neopustı́ jisté ...
To znamená, že v rovnovážné konfiguraci nabývá U stacionárnı́ (extremálnı́) hodnoty. Rovnovážná konfigurace se nazývá stabilnı́, jestliže pohyb vlivem malé poruchy
neopustı́ jisté ...
 Definice 4. Šroubový pohyb vzniká složenı́m rovnoměrného otáčivého pohybu kolem
pevné přı́mky (osy) a rovnoměrného posuvného pohybu ve směru této přı́mky. Šroubovice
je dráha bod...
Definice 4. Šroubový pohyb vzniká složenı́m rovnoměrného otáčivého pohybu kolem
pevné přı́mky (osy) a rovnoměrného posuvného pohybu ve směru této přı́mky. Šroubovice
je dráha bod...




