8/9 Reakce, vyroba a slouceniny halogenu
Transkript
TG – chemie – kvinta Ing. Ludmila Horká 8/9 Reakce, výroba a sloučeniny halogenů Halogeny ∙ ∙ ∙ ∙ se stoupajícím protonovým číslem Z klesá reaktivita halogen s nižším Z oxiduje z halogenidů halogen s vyšším Z (2KBr + Cl2 2KCl + Br2 ) halogen s vyšším Z redukuje z kyslíkatých solí halogen s nižším Z (I2 +2NaClO3 2NaIO3 +Cl2 ) příprava – oxidace halogenidů ∙ MnO2 + 4HCl Cl2 + MnCl2 + 2H2 O; 2Br – + Cl2 Br2 + 2Cl – ∙ výroba – elektrolýza vodného roztoku NaCl Bezkyslíkaté sloučeniny halogenů 1) halogenovodíky (halogenkyseliny) ∙ páchnoucí bezbarvé plyny, silné kyseliny a) HF kyselina fluorovodíková, vysoce toxická, žíravá kapalina, silně leptavé účinky na kůži; používá se k leptání skla a při výrobě matového skla (uchovává se v plastových nádobách) ∙ HCl kyselina chlorovodíková; příprava např. reakcí kyseliny sírové s NaCl; vznikající plynný HCl se rozpouští ve vodě na kyselinu; výroba hořením H2 s Cl2 a následným rozpouštěním HCl ve vodě; bezbarvá těkavá kapalina, žíravina, dodává se jako 37 % vodný roztok chlorovodíku, technická kyselina (kyselina solná) je nažloutlá kapalina, v lidském žaludku se vyskytuje pouze slabý (0,3 – 0,4%) roztok kyseliny ∙ na vzduchu silně dýmá, reaguje s kovy → H2 + Cl – ∙ SiO2 + 4HF SiF4 + 2H2 O; CaF2 + H2 SO4 CaSO4 + 2HF 2) vzájemné sloučeniny halogenů ∙ ochota slučovat se → stoupá se vzdáleností v PSP (BrF3 , IF5 , IF7 ) 3) halogenidy a) NaCl chlorid sodný (kuchyňská sůl, kamenná sůl) – doluje se nebo se získává odpařováním či vymrzáním mořské vody, v lidském těle je v slzách, v potu, v krvi, v moči, ve tkáňovém moku, v tělních tekutinách je 0,9 % chloridu sodného (stejné složení má fyziologický roztok); člověk přijímá s potravou asi 8-15 g soli denně (doporučená dávka je 4 g; nadbytek příjmu soli zvyšuje krevní tlak, kuchyňská sůl se jodiduje pro správnou funkci štítné žlázy; největší světovou zásobárnou chloridu sodného jsou moře a oceány, které obsahují i další soli – např. chlorid hořečnatý (dodává mořské vodě hořkou chuť) a chlorid draselný; celkový obsah solí rozpuštěných v mořské vodě je označován jako salinita (Baltského moře je 0,7-0,8 %, Černého moře 1,8 %, Jaderského moře 3,8 %, Rudého moře 4,2 %..., nejslanější je Mrtvé moře se salinitou 30 %), užití v potravinářství, konzervace, vysolování kůží, surovina pro výrobu Cl2 , H2 , NaOH (elektrolýzou roztoku chloridu sodného), výroba mýdel, sody b) KCl chlorid draselný – surovina pro výrobu jiných draselných solí, draselných (mazlavých) mýdel, hydroxidu draselného a draselných hnojiv c) NH4 Cl chlorid amonný, salmiak – pro čištění povrchu kovů při pájení, část suchých článků baterií d) AsCl3 chlorid arsenitý – prudký jed e) FeCl3 chlorid železitý – využití při úpravě pitné a užitkové vody v čističkách odpadních vod (váže na sebe nečistoty, po zatížení klesnou ke dnu; odstraní se usazením nebo filtrací) f) bromidy amonný, draselný, sodný – využívají se v lékařství jako sedativa g) bromidy stříbrný, vápenatý – využití ve fotografickém průmyslu h) CaF2 fluorid vápenatý, nerost fluorit, kazivec – využití v optice a pro výrobu kyseliny fluorovodíkové 4) hydrogenfluoridy – K[HF2 ], K2 [HgI4 ] Nesslerovo činidlo – pro důkaz NH3 Kyslíkaté sloučeniny halogenů 5) oxidy ∙ od Cl → plyny (Cl2 O7 = olejovitá kapalina) ∙ I2 O5 = nejstálejší (bílá krystalická látka 6) oxokyseliny ∙ od Cl → s počtem kyslíků stoupá síla kyseliny (nejslabší je HClO (ničí mikroorganismy, pro desinfekci vody, součást pracích, čistících a bělících prostředků), silnější je HClO2 , HClO3 a nejsilnější je HClO4 ), ale klesá stálost jejich solí ∙ od Br → HBrO, HBrO3 ∙ od I → HIO3 , H5 IO6 (bezbarvá krystalická látka) 7) soli ∙ od HClO4 → pro pyrotechniku, pohon raket ∙ od HClO3 KClO3 Travex proti plevelům (totální herbicid), pro zápalky a třaskaviny, ohňostroje, zábavní pyrotechnika ∙ od HClO2 NaClO2 oxidační činidlo → rozkládá se teplotou ∙ od HClO NaClO oxidační činidlo, bělení, desinfekční prostředky (např. Savo)
Podobné dokumenty
Halogeny a jejich sloučeniny
 Ve vodném roztoku tvoří vodíkové můstky. (Má tedy vyšší teplotu varu než ostatní HX.)
Leptá sklo: HF SiO
SiF
H O.
Na vzduchu velmi dýmá a její páry jsou mimořádně silně jedovaté.
Ve vodném roztoku tvoří vodíkové můstky. (Má tedy vyšší teplotu varu než ostatní HX.)
Leptá sklo: HF SiO
SiF
H O.
Na vzduchu velmi dýmá a její páry jsou mimořádně silně jedovaté.
vzorové příklady
 Takže molární hmotnost thiosíranu je 158,12 g.mol-1. Jinými slovy – jeden mol thiosíranu
sodného má hmotnost 158,12 g. Dále je potřeba zjistit, kolikrát se hmotnost jednoho molu
thiosíranu vejde do...
Takže molární hmotnost thiosíranu je 158,12 g.mol-1. Jinými slovy – jeden mol thiosíranu
sodného má hmotnost 158,12 g. Dále je potřeba zjistit, kolikrát se hmotnost jednoho molu
thiosíranu vejde do...
Úpravy chemických rovnic – procvičování (kvinta + 1.G)
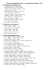 32. 2 KMnO4 + 5 H2O2 + 3 H2SO4 2 MnSO4 + K2SO4 + 5 O2 + 8 H2O
33. 2 KMnO4 + 5 HNO2 + 3 H2SO4 2 MnSO4 + K2SO4 + 5 HNO3 + 3 H2O
34. K2Cr2O7 + 3 H2S + 4 H2SO4
Cr2(SO4)3 + K2SO4 + 3 S + 7 H2O
35. 3 HgS...
32. 2 KMnO4 + 5 H2O2 + 3 H2SO4 2 MnSO4 + K2SO4 + 5 O2 + 8 H2O
33. 2 KMnO4 + 5 HNO2 + 3 H2SO4 2 MnSO4 + K2SO4 + 5 HNO3 + 3 H2O
34. K2Cr2O7 + 3 H2S + 4 H2SO4
Cr2(SO4)3 + K2SO4 + 3 S + 7 H2O
35. 3 HgS...
1/9 Přehled rovnic
 4 H2 + Si(OH)4
2 H2 O
2 H2 + O2 (elektrolýza)
C + H2 O
CO + H2 (směs CO a H2 je vodní plyn)
CO + H2 + H2 O (g) → CO2 + 2H2 (vodní plyn + vodní pára při 300∘ C s katalyzátorem)
CH4
C + 2 H2 ; CH4 + ...
4 H2 + Si(OH)4
2 H2 O
2 H2 + O2 (elektrolýza)
C + H2 O
CO + H2 (směs CO a H2 je vodní plyn)
CO + H2 + H2 O (g) → CO2 + 2H2 (vodní plyn + vodní pára při 300∘ C s katalyzátorem)
CH4
C + 2 H2 ; CH4 + ...
stanovení amonných iontů Nesslerovou metodou
 zbarvení. Chyba se eliminuje poté tak, že při stanovení absorbance vzorku zjištěné při
stanovení amoniakálního N, se odečte absorbance slepého stanovení vzorku, kde byl místo
Nesslerova činidla při...
zbarvení. Chyba se eliminuje poté tak, že při stanovení absorbance vzorku zjištěné při
stanovení amoniakálního N, se odečte absorbance slepého stanovení vzorku, kde byl místo
Nesslerova činidla při...
Zákon zachování hmotnosti
 a) 2KBr + Cl2 ---> 2KCl + Br2
b) 4HCl + MnO2 ---> Cl2 + MnCl2 + 2H2O
c) 4HI + O2 ---> 2H2O + 2I2
d) 3N2O + 2NH3 ---> 4N2 + 3H2O
a) 2KBr + Cl2 ---> 2KCl + Br2
b) 4HCl + MnO2 ---> Cl2 + MnCl2 + 2H2O
c) 4HI + O2 ---> 2H2O + 2I2
d) 3N2O + 2NH3 ---> 4N2 + 3H2O
přehled triviálních a mineralogických názvů - E
 Wolframan železnatomanganatý
Sulfid železnatý
Disulfid železnatý
Heptahydrát síranu
železnatého
Titaničitan železnatý
Wolframan gallnatý
Kyselina sírová
Kyselina
trihydrogenboritá
Wolframan železnatomanganatý
Sulfid železnatý
Disulfid železnatý
Heptahydrát síranu
železnatého
Titaničitan železnatý
Wolframan gallnatý
Kyselina sírová
Kyselina
trihydrogenboritá

 pokud je v názvu obsažen prvek a vodík, napíšu ve vzorci pouze tyto prvky (jedná se o bezkyslíkatou kyselinu),
vodík stojí vždy ve vzorci na prvním místě. Jedinou výjimkou je kys. sirovodíková, t...
pokud je v názvu obsažen prvek a vodík, napíšu ve vzorci pouze tyto prvky (jedná se o bezkyslíkatou kyselinu),
vodík stojí vždy ve vzorci na prvním místě. Jedinou výjimkou je kys. sirovodíková, t...

